Un acide aminé ou amino-acide est un composé organique possédant à la fois une fonction carboxylique $\rm -CO_2H$ et une fonction aminé $\rm -NH_2$.
Un acide $\alpha-$aminé est un acide carboxylique dans lequel le groupe amino est porté par l'atome de carbone en $\alpha$ du groupe carboxyle.
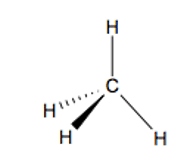
La formule générale des acides $\alpha-$aminés naturels est :
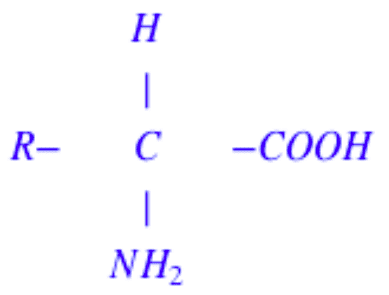
Où $\rm R$ peut être un atome d'hydrogène, un groupe alkyle linéaire.
Les acides aminés sont des espèces amphotères. Elles sont donc caractérisées par deux $\rm pK_A$.
$\rm H_3N^+- CHR-COOH \leftrightharpoons H_3N^+ CHR - COO- + H^+$
Couple : $\rm (H_3N^+-CHR-COOH / H_3N^+-CHR-COO^-) : pK_{A1}$
$\rm H_3N^+- CHR-COO^- \leftrightharpoons H_2N - CHR-COO^- + H^+$
Couple : $\rm (H_3N^+-CHR-COOH / H_3N^+-CHR-COO^-) : pK_{A2}$
Propriété acido-basiques des acides aminés
Les acides aminés possèdent à la fois un groupe acide $\rm -COOH \:(R-COOH / R-COO^-)$ et un groupe basique $\rm -NH_2\:(R-NH_3^+ / R-NH_2)$. En solution aqueuse, la structure d'un acide aminé dépend donc de la valeur du pH.
Exemple :
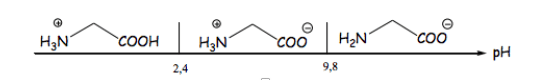
Pour la glycine :
$\rm -COOH / -COO \::\:pK_{a1} = 2,4$
$\rm -NH_3^+ / -NH_2 \: : \: pK_{a2} = 9,8$
Liaison peptidique
Les acides aminés donnent ieu à une grande diversité de combinaisons en biologie parce que ceux-ci peuvent se polymériser : on forme ainsi des polypeptides. De tels polymères se forment à la suite de réactions répétées de la fonctiona acide carboxylique d'un acide aminé avec le groupe amino d'un autre ce qui aboutit à l'élaboration d'une chaîne d'amides. Le lien amide qui unit des acides aminés est appelé liaison peptidique.
Exemple de dipeptide
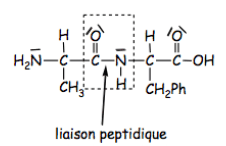
Ce dipeptide est obtenu par condensation de deux acides aminés : l'alanine et la phénylalanine.