Un électrolyseur est un récepteur électrique qui convertit de l'énergie électrique en énergie chimique.
Un électrolyseur est constitué d'un récipient, de deux électrodes conductrices, qui trempent dans une solution contenant des ions.
Parmi ces constituants, se trouvent au moins un oxydant $\rm Ox_1$ (couple : $\rm Ox_1 / Red_1$) et un réducteur $\rm Red_2 (couple Ox_2 / Red_2).$
Au cours de l'électrolyse a lieu une réaction d'oxydoréduction non spontanée, dite forcée entre l'oxydant $\rm Ox_1$ qui se réduit à l'électrode reliée à la borne négative du générateur, la cathode, et le réducteur $\rm Red_2$, qui s'oxyde à l'électrode reliée à la borne positive du générateur, l'anode.
La réduction de $\rm Ox_1$ peut avoir lieu grâce à l'apport des électrons fournis par la borne négative du générateur.
On a une réduction à la borne négative : $\rm Ox_1 + n_1 e^-$ = $\rm Red_1$ et une oxydation à la borne positive : $\rm Red_2$ = $\rm Ox_2 + n_2 e^-$.
Quand l’électrolyseur fonctionne, on a donc la réaction d’oxydoréduction :
$\rm n_2 Ox_1 + n_1Red_2\rightarrow n_1 Ox_2 + n_2Red_1$.
L'électrode de l'électrolyseur reliée à la borne positive du générateur, sur laquelle a toujours lieu l'oxydation du réducteur est appelée anode, l'électrode reliée à la borne négative, sur laquelle a toujours lieu la réduction de l'oxydant, cathode.
I (en A), l'intensité du courant débité par le générateur est :
I = $Q / \Delta t$ = $\rm (n(e^-) _{éch} \times F)/ \Delta t$ :
avec :
- Q (en C), la quantité d'électricité mise en jeu au cours de l'électrolyse pendant la durée de fonctionnement $\rm \Delta t$ (en s),
- $n(e^-)_{éch}$ (en mol), la quantité d'électrons échangés, pendant la durée $\Delta t$, au cours de la réaction d'oxydoréduction d'électrolyse,
- F, la constante de faraday : $\rm F = 96 500 C.mol^{-1}$.
Exemple :
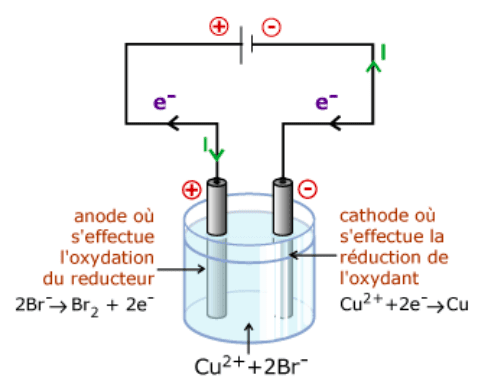
Au cours de l'électrolyse d'une solution de bromure de cuivre (II) :
- à la cathode, l'électrode de carbone reliée à la borne négative du générateur, l'oxydant $\rm Cu^{2+}$, présent dans la solution dans laquelle trempe les électrodes de carbone, se réduit selon : $\rm Cu^{2+} + 2 e^- \rightarrow Cu$, en captant les électrons fournis par le générateur ;
- à l'anode, l'électrode de carbone reliée à la borne positive du générateur, le réducteur $\rm Br^-$s'oxyde en $\rm Br^2$ selon : $\rm 2 Br^-\rightarrow Br_2 + 2 e^-$.
On a alors :
$\rm 2 Br^-(aq) + Cu^{2+}(aq)\rightarrow Br_2(aq)+ Cu(s)$.