Changements d'état des corps purs
Quand un corps pur (un échantillon de matière unique) change d'état, ce changement s'effectue :
- À température constante
- En conservant sa masse
Identification expérimentale des changements d'état
Expérimentalement, il est possible de tracer la courbe de la température d'un échantillon en fonction du temps pendant qu'il est réchauffé ou refroidi. Nous pouvons donc identifier le moment où il change d'état quand nous observons un palier de température au niveau de la courbe.
Visuellement, le changement d'état se situe au moment où nous observons que la matière se trouve dans les deux états simultanément.
Solidification de l'eau pure
Exemple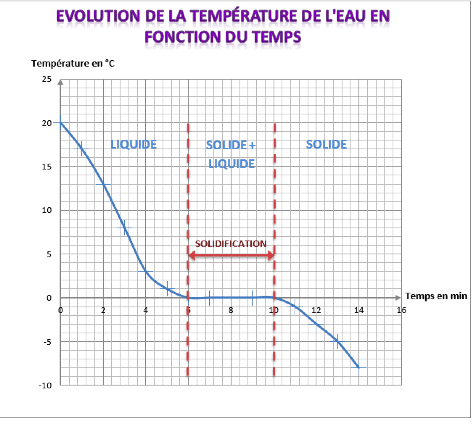
Comparaison avec les mélanges
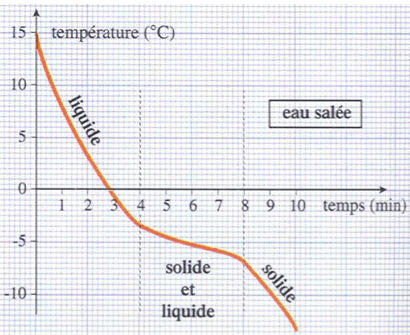
En comparaison, l'eau salée (qui n'est pas un corps pur mais un mélange eau-sel), ne présentera pas de palier, mais un changement de pente seulement.
Solidification de l'eau salée
Exemple